we discover ...
ÜBER UNS Biotracing
ÜBER UNS
Der Wirtschaftsstandort Bremerhaven bietet als Tor zur Welt genau die Art von kosmopolitischer Weltoffenheit, die die Firma mir|detect für die Konzentration auf ihre Arbeit benötigt.
Krebs ist ein internationales Thema. Viele Krebsarten sind nicht ausreichend erforscht.
mir|detect schafft Klarheit und Sicherheit
nicht nur im Bereich "Hodenkrebs".
mir|detect: Biotechnologie aus Bremerhaven.
TEAM Biotracing













HISTORIE Biotracing
HISTORIE
M371-Test
CE Zertifizierung nach IVDR
(In vitro Diagnostic Medical Device Regulation)
M371-Test auf zwei neuen qPCR-Plattformen validiert
Studie zur Wirksamkeit des M371-Test in der Nachsorge veröffentlicht.
Exklusiver Vertriebsvertrag für Europa
mit Gold Standard Diagnostik
Präsentation von
M371-Test
auf der DGU in Stuttgart
Zertifizierung nach ISO 13485
CE Zertifizierung nach IVDD
Finalist des
EIT Health Headstart Förderprogramms 2019
Nominierung für den
ACHEMA-Gründerpreis 2018
Präsentation des Serummarkers miR-371a auf der
9th Copenhagen Workshop on Testikular Germ Cell Cancer
Auszeichnung durch
Sience4Life Cup 2017
Finalist im
BioVaria-Kongress 2017 in München
Auszeichnung:
Venture Lounge 2016
Gründung der mir|detect GmbH
Projekt an der
Universität Bremen
AKTUELLES Biotracing
Archiv | 2021
4. April 2024
ZERTIFIZIERUNG
Erfolgreiche CE2797-Zertifizierung von M371-Test nach IVDR
Der von mir|detect entwickelte M371-Test zum Nachweis und Monitoring von testikulären Keimzelltumoren besitzt seit April 2024 die Zulassung gemäß Verordnung 2017/746 IVDR und erhält damit eines der ersten IVDR-Zertifikate in der EU.
Die neue EU-Verordnung verschärft die regulatorischen Vorgaben im Vergleich zur Richtlinie 98/79/EC IVDD signifikant und sorgt für mehr Sicherheit für Patienten und Anwender in der Nutzung von In-vitro-Diagnostika.
Mit der IVDR-Zertifizierung von M371-Test ist gewährleistet, dass die wissenschaftliche Validität sowie die analytische und klinische Leistungsfähigkeit von unabhängiger Stelle ausführlich geprüft und bestätigt wurde.

3. März 2024
NEUE CYCLER
Hervorragende diagnostische Leistung des M371-Test auf neuen qPCR-Plattformen
mir|detect hat den M371-Test zur Erkennung von Keimzelltumoren des Hodens für den Einsatz auf zwei neuen qPCR-Plattformen validiert:
- AriaDx (Agilent)
- QuantStudio 5 (ThermoFisher Scientific)
Der M371-Test bietet auf beiden Geräten die gleiche exzellente, diagnostische Leistung wie auf dem LightCycler 480 II und erhöht somit die Zugänglichkeit für Labore und damit die Zahl der Patienten, die durch den M371-Test profitieren.
Weiterhin arbeitet mir|detect mit Hochdruck an der Validierung des M371-Test auf dem LightCycler PRO (Roche) und dem CFX96 (Bio-Rad) um den M371-Test vielen Patienten und Anwendern zugänglich zu machen.
15. Januar 2024
NACHSORGESTUDIE
Hervorragende diagnostische Leistung des M371-Test auf neuen qPCR-Plattformen
Der M371-Test bietet Ihnen eine beispiellose diagnostische Genauigkeit und ermöglicht einen bahnbrechenden Ansatz für die Behandlung von Hodenkrebs. Eine richtungsweisende Studie hat die Wirksamkeit von M371-Test von mir|detect bei der Erkennung von Rezidiven von Keimzelltumoren des Hodens bestätigt.
Die frühzeitige Erkennung von Rezidiven ist bei der Nachsorge von Patienten mit testikulären Keimzelltumoren von entscheidender Bedeutung. In einer kürzlich veröffentlichten Studie wurden die Serumspiegel der miR-371a-3p bei 258 Patienten mit dem M371-Test von mir|detect überwacht. Während der Nachbeobachtung traten 39 Rückfälle auf. In allen diesen Fällen wurden erhöhte Spiegel der miRNA nachgewiesen, was einer Sensitivität und Spezifität von 100 % bzw. 96,3 % entspricht. Damit übertrifft die miR-371a-3p die klassischen Serummarker deutlich.
Diese Ergebnisse unterstreichen die Eignung von M371-Test von mir|detect für die Erkennung von Rezidiven, und der Test stellt somit einen deutlichen Fortschritt in der Nachsorge von Hodenkrebspatienten dar.
Die Arbeit wurde in Clinical Cancer Research veröffentlicht und ist jetzt online verfügbar: https://doi.org/10.1158/1078-0432.ccr-23-0730
12. Mai 2023
VERTRIEBSTAGUNG
Gold Standard Diagnostik zu Besuch in Bremerhaven
Am 12. Mai 2023 erhielten wir Besuch eines Teams unseres exklusiven Vertriebspartners Gold Standard Diagnostik in unseren Räumen in Bremerhaven.
Wir sind stolz darauf, den im November 2022 eingeschlagenen Weg mit diesem europaweit gut vernetzten und etablierten Partner fortzugehen und freuen uns auf eine weitere intensive und fruchtbare Zusammenarbeit.

April 2023
VENTURE CAPITAL MAGAZIN
Neuer Goldstandard


21. - 23. September 2022
DGU HAMBURG
74. Deutsche Gesellschaft für Urologie
Über drei Tage präsentiere mir|detect auf dem firmeneigenen Messestand den Test M371 auf dem Kongress der Deutschen Gesellschaft für Urologie und stand für interessierte Fragen zur Verfügung.
Herr Prof. Dr. Klaus-Peter Dieckmann teilte seine neusten Erkenntnisse zur miRNA-371a im Rahmen des wissenschaftlichen Programms mit Kollegen.



19. & 20. Mai 2022
UROBAY LINDAU
48. Tagung der Bayrischen Urologenvereinigung und der Österreichischen Gesellschaft für Urologie
mir|detect präsentierte auf dem firmeneigenen Messestand den Test M371.



20. & 21. April 2022
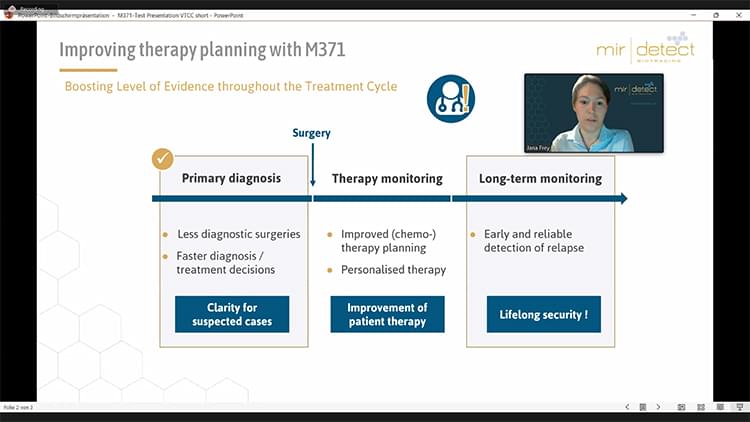
VIRTUAL TESTICULAR CANCER CONFERENCE
Testicular Cancer Awareness Foundation
mir|detect war Platinum Sponsor der Konferenz.
Frau Jana Frey ( Produkt Management ) sprach für mir|detect auf dem virtuellen Treffen.

7. Oktober 2021
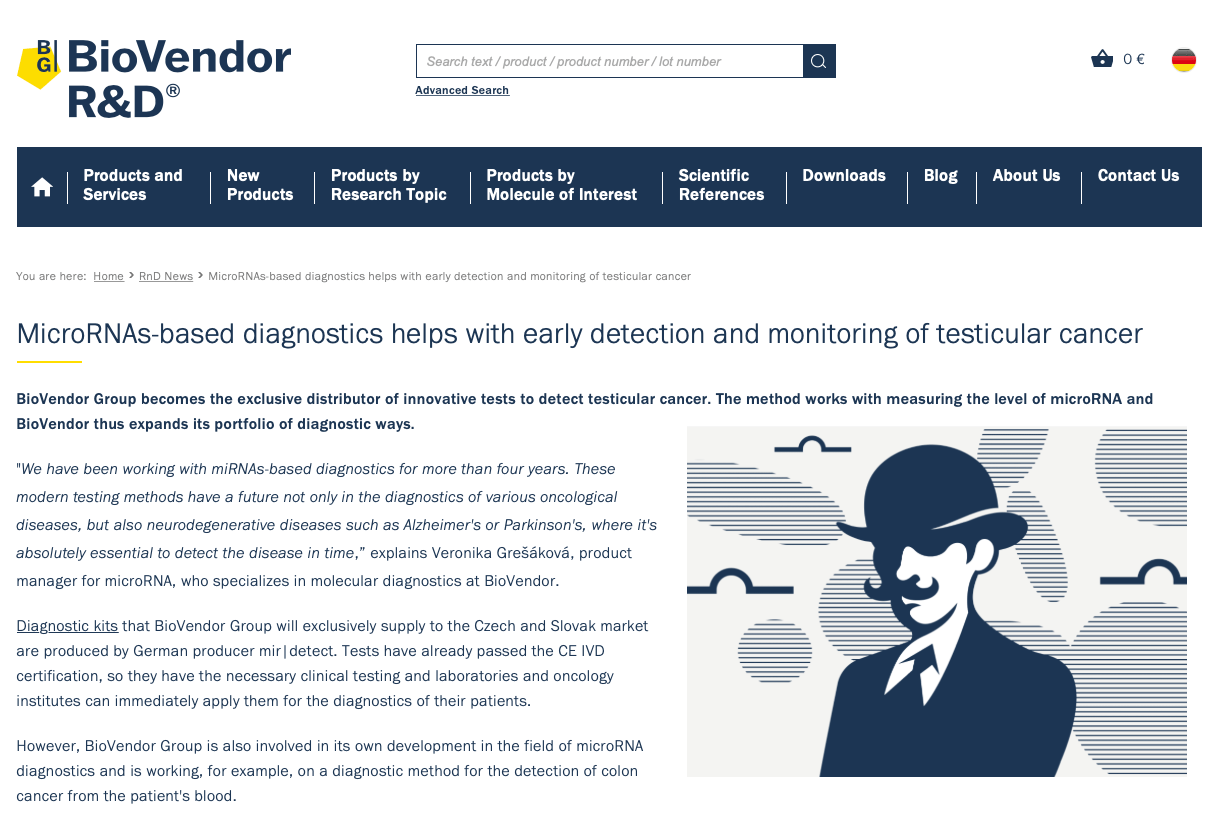
PRESSEMITTEILUNG:
BioVendor | Laboratorni medicina a.s. | Tschechien
M371 kann nun über BioVendor in Brno bezogen werden.
zur Pressemitteilung
15. - 18. September 2021
DGU KONGRESS STUTTGART
Deutsche Gesellschaft für Urologie
mir|detect präsentierte M371 auf dem Deutschen Urologie Kongress
Interessenten konnten Ihre Fragen direkt an das mir|detect-Team stellen.



15. Juni 2021
PRESSEMITTEILUNG:
GeLaMed | Eurofins Laborbetriebsgesellschaft Gelsenkirchen GmbH
M371 ist nun über das Eurofins Labor in Gelsenkirchen (GeLaMed) erhältlich.
Die Anwendung des Tests erfolgt beim behandelnden Urologen.
zur Pressemitteilung

KARRIERE Biotracing
Stellenangebote
Derzeit bieten wir keine offenen Stellen.
Wir haben hier Inhalte von OpenStreet Map eingebettet. Da OpenStreet Map möglicherweise personenbezogene Daten sammelt und Ihr Benutzerverhalten analysiert, laden wir die Karte nur, nachdem Sie der Verwendung von Cookies und ähnlichen Technologien gemäß unserer Datenschutzrichtlinie zugestimmt haben.